Études de PK
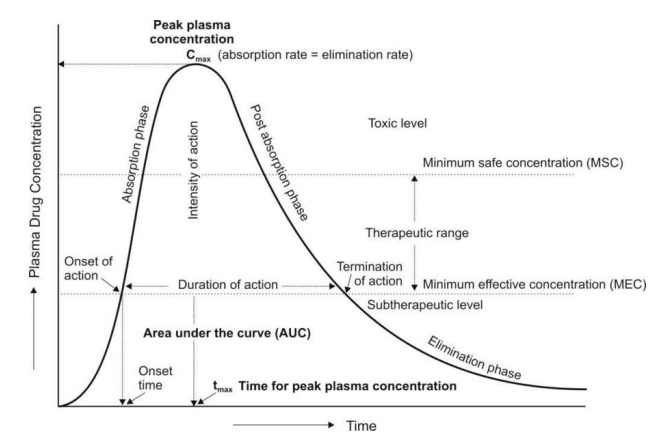
Les études de pharmacocinétique (PK) sont essentielles en recherche préclinique. Elles décrivent le comportement et le devenir d’un composé dans un organisme, fournissant des données cruciales pour évaluer la sécurité et l’efficacité d’un médicament lors des essais cliniques.
Voici quelques avantages clés des études PK en recherche préclinique :
- Identifier les risques de toxicité : Les études PK peuvent révéler des risques potentiels liés à un médicament, comme la toxicité ou les interactions médicamenteuses, contribuant à la conception d’essais cliniques plus sûrs.
- Déterminer le dosage optimal : Les études PK aident à établir la posologie optimale d’un médicament, comme la dose, la fréquence et la voie d’administration, données cruciales pour obtenir l’effet thérapeutique souhaité chez les patients.
- Prédire la PK chez l’humain : Les études PK chez l’animal servent à prévoir le comportement d’un médicament chez l’homme, des données utiles pour la conception et l’interprétation des essais cliniques.